اطلاعات زمینه ای
بیمارانیکه به دنبال بی حرکتی دچار التهاب سیاهرگ های پا میشوند (ترومبوفلبیت) ویا افرادی که تحت عمل جراحی برروی لگن یا شکم قرار میکیرند مستعد لخته شدن خون در ریه ها هستند که آمبولی ریه نامیده میشود و باید بلافاصله تشخیص داده شده و تحت درمان قرارگیرد. تشخیص آمبولی ریه با استفاده از این اسکن است. برای انجام این اسکن آمادگی خاصی لازم نیست. بیمار زیر دستگاه خوابیده و بعد از تزریق پرتو دارو اسکن در نماهای مختلف به عمل می آید.
این اسکن جهت بررسی خونرسانی نسج ریه بکار می رود. هر عاملی که باعث کاهش خونرسانی نسج ریه شود، به صورت نقص پرفیوژن در اسکن مشاهده خواهد شد. از شایع ترین کاربردهای آن اثبات یا رد آمبولی ریه در بیمارانی می باشد که به دنبال اعمال جراحی، دچار علائم حاد تنفسی می شوند. معمولاً اسکن پرفیوژن ریه در این موارد به همراه اسکن ونتیلاسیون ریه انجام می شود ولی در اغلب مراکز به دلیل موجود نبودن رادیو داروی مناسب برای اسکن ونتیلاسیون ریه، اسکن پرفیوژن به تنهایی و مقایسه آن با رادیوگرافی ساده ریه از دقت تشخیصی قابل قبولی برخوردار می باشد. کاربرد دیگر آن بررسی کمّی میزان پرفیوژن هر یک از لوب ها و یا سگمان های ریه می باشد که قبل از عمل جراحی برداشتن قسمتی از ریه، از اهمیت قابل توجهی برخوردار است. این اسکن نیاز به آمادگی خاصی ندارد و تصویربرداری بلافاصله بعد از تزریق انجام می شود.
قبل از انجام اسکن ریه لازم است رادیوگرافی قفسه سینه و تستهای انعقاد خونی (بویژه (D-Dimerانجام شود. ترجیح دارد که رادیوگرافی معمول ریه را در نمای خلفی- قدامی (PA) و نیمرخ گرفت. فقط در صورتیکه بیمار نتواند وضعیت معمول رادیوگرافی قفسه سینه را تحمل کند، رادیوگرافی پرتابل قدامی- خلفی (AP) قفسه سینه قابل قبول است. در صورتیکه علائم و نشانه های بیمار تغییری نکند، انجام رادیوگرافی قفسه سینه در فاصله یک روز از اسکن کفایت می کند. در بیمارانی که نشانه و علائم متغیر می باشد، یک رادیوگرافی بسیار جدید (ترجیحا در فاصله یک ساعت) ضرورت دارد.
نحوه و ترتیب تصویربرداری
قبل از اینکه پرتوداروی پرفوزیون ریه را به صورت وریدی تجویز نمود، باید به بیمار باید تذکر داد سرفه کند و چند نفس عمیق بکشد. بیمار باید در حین تزریق در وضعیت طاقباز و در مواردی که تنگی نفس دارد، در حد امکان نزدیک به طاقباز باشد. پس از تزریق وریدی رادیو داروی مناسب در حالی که بیمار بر روی تخت دراز کشیده، تصاویر از زوایای مختلف از ناحیه قفسه سینه جهت بررسی نحوه توزیع رادیو دارو در ریه ها، گرفته می شود. اسکن پرفیوژن ریه حدود ۱۵-۲۰ دقیقه طول خواهد کشید.
الف) سنتی گرافی ونتیلاسیون با آئروسل ( DTPA m99-(Tc یک آزمون تصویربرداری تشخیصی است که توزیع آئروسل رادیواکتیو استنشاقی را در ریه ها ثبت می کند. آئروسل با یک دهنی و با بینی بسته تجویز شده و بیمار تنفس جاری (tidal) را انجام می دهد.
ب) سنتی گرافی پرفوزیون ریوی MAA) m99-Tc) یک آزمون تصویربرداری تشخیصی است که توزیع جریان خون شریان ریوی را پس از تزریق وریدی رادیودارو ثبت می کند. بعد از سرفه کردن بیمار و چند نفس عمیق، MAA m99- Tc را به آهستگی در عرض ۵ سیکل تنفسی تزریق نمود در حالیکه بیمار در حالت طاقباز قرار دارد.
ت) سنتی گرافی ریه برای آمبولی ریه یک آزمون تصویربرداری تشخیصی است که پرفوزیون ریوی را ارزیابی می کند و معمولا شامل سنتی گرافی ونتیلاسیون نیز می باشد.
کاربردهای شایع
الف) شایعترین کاربرد سنتی گرافی ریه، تعیین احتمال آمبولی ریه است.
ب) کاربرد کم اهمیت تر آن (مانند ارزیابی پیوند ریه، ارزیابی قبل از عمل، ارزیابی شانت راست به چپ).
آمادگی بیمار
جهت انجام اسکن آمادگی خاصی لازم نیست. ولی چون مقایسه اسکن با رادیوگرافی ریه ها ضروری است، بهتر است بیمار رادیوگرافی جدید خود را همراه داشته باشد.
اطلاعات زمینه ای
یکی از بیماری های خاموش اما آزار دهنده به خصوص در سنین میانسالی، پر کاری پاراتیروئید می باشد که متأسفانه تشخیص صحیح آن اغلب به تأخیر می افتد و بیمار با عوارض جبران ناپذیری دست به گریبان خواهد بود. تشخیص اولیه پر کاری پاراتیروئید با آزمایشات خون صورت می گیرد اما با توجه به اینکه چهار عدد غده پاراتیروئید در جلوی گردن در اطراف غده تیروئید قرار دارند، گاهی یافتن مکان دقیق غده درگیر مشکل می باشد که با انجام اسکن پاراتیروئید، مکان غده درگیر به خوبی شناسایی می شود. هیپرپاراتیروئیدیسم اولیه عبارت است از افزایش تولید و رها شدن هورمون پاراتیروئید که سبب افزایش سطح کلسیم سرم و کاهش سطح فسفاتهای معدنی می شود. بیمار بدون علامت، غالبا از طریق غربالگریطی بررسی آزمایشات شیمی خون با روش اتوماتیک شناخته می شود. علت هیپرپاراتیروئیدیسم اولیه در اکثر موارد (۸۵%-۸۰%)، آدنوم پرکار منفرد یا متعدد می باشد. هیپرپلازی چند یا همه غدد پاراتیروئید در ۱۵%-۱۲% موارد و کارسینوم پاراتیروئید فقط در ۳%-۱% موارد هیپرپاراتیروئیدیسم اتفاق می افتد. به طور کلی از نظر سنتی گرافی می توان پاراتیروئید بزرگتر از mg 500 را تشخیص داد. اخیرا پرتوداروی Tc-99m sestamibi، تشخیص غدد هیپرپلاستیک را میسر نموده است، اگرچه در مقایسه با تشخیص آدنوم، حساسیت آن کمتر می باشد.
فرآیند معمول انجام اسکن
برای انجام این اسکن ابتدا رادیو دارو به صورت وریدی تزریق می شود و در فواصل ۲۰ دقیقه، ۲ ساعت و گاهی ۴ ساعت از جلوی گردن و قفسه سینه بیمار تصویربرداری انجام می شود. گاهی لازم است اسکن تیروئید هم برای مقایسه با تصاویر اسکن پاراتیروئید انجام شود. همچنین گاهی به کار بردن روش SPECT برای افزایش دقت تشخیص ضرورت پیدا می کند.
کاربردهای شایع
الف) تعیین موقعیت بافت پرکار پاراتیروئید (آدنوم یا هیپرپلازی) در هیپرپاراتیروئیدیسم اولیه. قبل از عمل جراحی می توان با پیدا کردن ضایعه و در نتیجه کوتاه نمودن زمان عمل به جراح کمک نمود.
ب) تعیین موقعیت بافت پرکار پاراتیروئید (معمولا آدنوم) در بیماران مبتلا به بیماری مزمن و یا عودکننده. بسیاری از این بیماران سابقه یک یا چند عمل جراحی دارند که از نظر تکنیکی، جراحی مجدد را دشوار می سازد. همچنین در این جمعیت از بیماران، وجود بافت نابجا بسیار شایع است و این اسکن شانس موفقیت جراحی را افزایش می دهد.
نحوه اجرا
لف) آمادگی بیمار
آمادگی خاصی لازم نیست. بیمار باید در صورتی که باردار است کارشناس را مطلع نماید
اطلاعات قبل از انجام آزمون
۱- مدرک مربوط به افزایش سطح کلسیم سرم و هورمون پاراتیروئید.
۲- نتیجه معاینه فیزیکی به خصوص لمس گردن.
۳- وجود بیماری تیروئید همراه به خصوص تیروئید ندولار.
۴- تجویز اخیر ترکیبات حاوی ید از جمله در مطالعات رادیوگرافیک (شامل سی تی اسکن، اوروگرافی وریدی) یا هورمون تیروئید، هنگامی که تصویربرداری تیروئید و تکنیک تفریقی بعد از آن انجام می شود.
۵- نتیجه سی تی اسکن یا اولتراسوند و سایر آزمایشات تشخیصی.
این رادیو دارو در درمان سرطان تیروئید و پر کاری تیروئید مقاوم به درمان دارویی، کاربرد گسترده ای دارد و بر اساس مطالعات انجام شده در ۶۰ سال گذشته، عارضه جانبی قابل اهمیتی از آن مشاهده نشده است. قبل از تجویز ید، از بیمار خواسته می شود که به مدت ۴ ساعت ناشتا باشد و مصرف داروهای خاص را نیز قطع کند.
ید رادیواکتیو برای درمان سرطان تیروئید از قدیمی ترین و درمانی ترین ،ید است که برای درمان سرطان تیروئید تثبیت، وهمچنین برای طیف وسیعی از بیماری های خوش خیم تیروئید استفاده می شود. این درمان ها به خوبی وبا میزان موفقیت بالا تثبیت شده است.
درمان ید رادیواکتیو چیست؟
ید رادیواکتیو به عنوان یک رادیو دارو یکی از قدیمی ترین و موفق ترین درمان رادیونوکلئید ارائه شده در سراسر جهان است. جذب طبیعی تیروئید به ید اجازه می دهد تا درمان تیروئید که غیر تهاجمی است با استفاده از ید رادیواکتیو بسیار هدفمند. ید رادیواکتیو دارای ویژگی های همان ید موجود در مواد غذایی؛ با این حال با ید رادیواکتیو تابش است که آسیب رساندن به بافت را ساطع می کند. با ید رادیواکتیو است که معمولا به عنوان یک کپسول، بزرگتر از یک قرص پاراستامول معمولی داده شده است. همچنین می تواند به عنوان مایع مخلوط شده با آب تجویز شود. هنگامی که در جریان خون، تیروئید با ید رادیواکتیو برای تولید هورمون های T3 و T4 جذب می کند. تابش که توسط فرسایش ید رادیواکتیو (از بین می برد) به بافت اطراف آن داده می شود، تا زمانی که توسط تیروئید جذب می شود، آن را قادر به ارائه پرتو را به هدف محدود می سازد.
تیروئید قادر به جذب تمام ید رادیواکتیو به عنوان یک ظرفیت محدود نیست . این است که چرا قبل از هر درمان با ید رادیواکتیو، یا یک رژیم غذایی کم ید و یاتزریق لازم است برای افزایش تحریک کننده تیروئید هورمون (TSH) برای حداکثر جذب از ید رادیواکتیو در زمان دو تیروئید قادر به جذب تمام ید رادیواکتیو به عنوان یک ظرفیت محدود نیست. این که چرا قبل از هردرمان با ید رادیواکتیو، یا یک رژیم غذایی کم ید و یاتزریق برای افزایش تحریک کننده تیروئید هورمون (TSH) برای حداکثر جذب از ید رادیواکتیو، زمان لازم است. تیروئید ی که ید جذب نمی کند به خارج از خون فیلتر شده و دفع عمدتا از نه طریق ادرار، بلکه از طریق سایر مایعات بدن مانند عرق و بزاق انجام می شود. به منظور به حداقل رساندن تابش اشعه به دیگرقسمت های بدن بیماران، تقاضا به نوشیدن مقدار زیادی مایعات و همچنین ادرار کردن ودوش به طور منظم می شود.
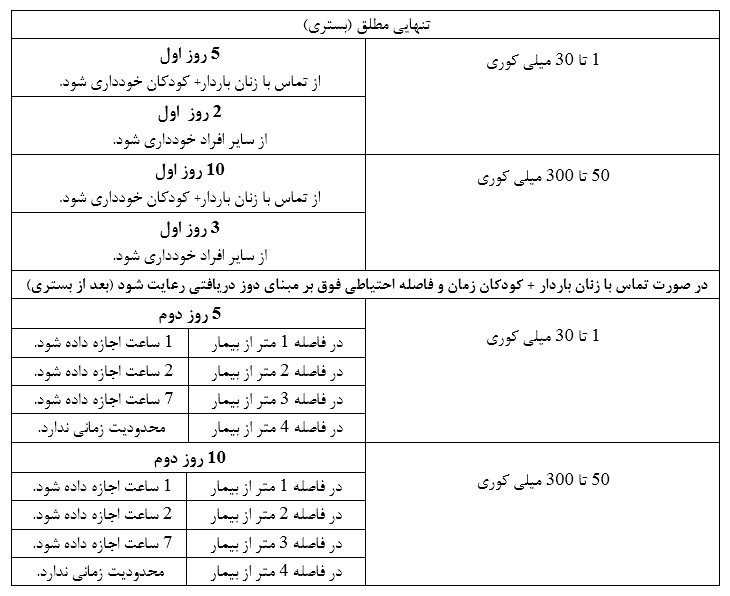
مشاوره حفاظت از اشعه بسته به اندازه تجویز دوز، شامل اقدامات احتیاطی اما معمولی است که متفاوت می باشد.
– نزدیک (کمتر از طول بازو) و طولانی مدت (بیشتر از ۱۰ دقیقه) در تماس با کودکان زیر شش سال و زنان باردار به مدت هشت روز
– نزدیک (کمتر از طول بازو) و طولانی مدت (بیشتر از ۱۰ دقیقه) با بزرگسالان در تماس منظم (به عنوان مثال دوستان نزدیک، اعضای خانواده) به مدت سه روز
– به اشتراک گذاری تخت به مدت پنج روز
این اقدامات احتیاطی به طور معمول می تواند به یک برنامه روزانه بدون مانع بسیار خوب تبدیل شود.
یک فیزیکدان پزشکی می تواند اقدامات احتیاطی معمول قبل از درمان را تجویز کند.
پروتکل تیروژن:
درمان قطع شیردهی در بیماران قبل از دریافت کننده ید رادیواکتیو:
از آگونیست دوپامین مانند قرص Cabergoline توصیه می شود (مجموعا” چهار عدد قرص) استفاده کنید:
- یک عدد امروز و یک عدد فردا
- یک هفته بعد هم مجددا” یک قرص در دو روز متوالی
دو ماه پس از قطع کامل شیردهی، بیمار را با قطع لووتیروکسین و در صورت لزوم تزریق تیروژن آمادگی بدهید و با تایید TSH بالای ml/mIU30 ید را تجویز فرمایید.
مشاوره حفاظت از اشعه بسته به اندازه تجویز دوز دریافتی، زمان و فاصله مجاز از اطرافیان متفاوت می باشد.
مطلب مرتبط با اسکن سر و گردن: اسکن تیروئید
کاربرد رادیودارویI-131 MIBG در درمان تومورهای با منشا غددی- عصبی، خصوصا از نوع نورواکتودرمال (سمپاتوآدرنال) شامل فئوکروموسیتوم، پاراگانگلیوم و نوروبلاستوم موثر بوده است. در سایر تومورهای غددی- عصبی (عمدتا کارسینوئید و کارسینوم مدولاری تیروئید) نیز این درمان گاهی می تواند موثر واقع گردد. استفاده ازI-131 MIBG برای تومورهای فئوکروموسیتوم و پاراگانگیوم کارآمدترین روش درمان غیرجراحی است، زیرا علاوه بر افزایش امید به زندگی، علایم بیمار را نیز به طور قابل ملاحظه ای (۹۰-۷۵ درصد) کنترل می کند. در نوروبلاستوم اگرچه در موارد با عود مکرر و مقاوم به درمان ۳۰ درصد تاثیر درمانی داشته است، اما با افزودن سایر مودالیتی های درمانی به این نوع درمان، موفقیت بیشتری به دست می آید، ضمن این که I-131 MIBG در کنترل علایم نیز موثر بوده است. برای سایر تومورهای غددی- عصبی شامل تومور کارسینوئید و کارسینوم مدولاری تیروئید اثرات این درمان در کاهش علائم بیمار مشاهده شده است. مهم ترین عارضه این درمان مهار مغز استخوان است که نیاز به پیگیری و درمان در صورت لزوم دارد I-131 MIBG نقش مهمی در درمان تومورهای کرومافینی دارد و برای تومورهای فئوکروموسیتوم و پاراگانگیوم کارآمدترین درمان غیرجراحی است.
درمان دردهای استخوانی با استرانسیوم ۸۹ (متاسترون) و ساماریوم ۱۵۳
یکی از عوارض ناتوان کننده بدخیمی ها، متاستازهای استخوانی و درد ناشی از آن است که بیشتر در سرطان پروستات و پستان دیده می شود. در کشورهای پیشرفته، یکی از درمان های رایج برای کاهش درد در متاستازهای گسترده استخوانی، استفاده از رادیو داروها نظیر استرانسیوم ۸۹ یا ساماریوم ۱۵۳می باشد. این درمان نیاز به بستری نداشته و به صورت سرپایی قابل انجام است. قبل از درمان، انجام اسکن استخوان جهت بررسی شدت و وسعت درگیری استخوانی لازم است. در حال حاضر در کشور ما علاوه بر متاسترون درمان با ساماریوم ۱۵۳ با هزینه کمتر و اثرات کاملاً مشابه در دسترس می باشد.
لازم به ذکر است که درمان درد های استخوانی با این رادیوایزوتوپها نیاز به بررسیهای اولیه خاصی داشته که توسط پزشک انجام می شود. پس از تجویز رادیودارو در ابتدا ممکن است دردهای بیمار بیشتر شود و سپس کاهش یابد.
مطلب مرتبط با اسکن تمام بدن: اسکن تمام بدن استخوان
این رادیو دارو در درمان سرطان تیروئید و پر کاری تیروئید مقاوم به درمان دارویی، کاربرد گسترده ای دارد و بر اساس مطالعات انجام شده در ۶۰ سال گذشته، عارضه جانبی قابل اهمیتی از آن مشاهده نشده است. قبل از تجویز ید، از بیمار خواسته می شود که به مدت ۴ ساعت ناشتا باشد و مصرف داروهای خاص را نیز قطع کند.
مطلب مرتبط با اسکن سر و گردن: اسکن تیروئید
سینوویورتز رادیواکتیو که با تزریق رادیوایزوتوپهای بیضرر به داخل مفاصل مبتلا به آرتریت مزمن صورت میگیرد، از جمله روشهای جدید در درمان آرتروپاتی هموفیلیک محسوب میگردد. این روش درمانی که با هدف اولیه کاهش همارتروز و مصرف فاکتور انعقادی به کار رفته است، میتواند تاثیر بهسزایی در بهبود کیفیت زندگی و کاهش بار اقتصادی ناشی از مصرف فاکتور انعقادی داشته باشد. سینوویورتز با فسفر رادیواکتیو، میتواند روشی مؤثر و به صرفه در کاهش همارتروز و مصرف فاکتور در بیماران مبتلا به آرتروپاتی هموفیلیک باشد.
مطلب مرتبط با اسکن تمام بدن: اسکن استخوان سه فاز
درمان متازستازهای کبد با امبولیزاسیون شریان تغذیه ای تومور
میکروسفرها
میکروسفرها، حوزه های رزین های کوچک است که حاوی صدها ذرات رادیونوکلئید هستند، که یک سبک درمانی براکی تراپی رادیونوکلئید است که برای درمان سرطان های کبد ایجاد شده است. ماهیت نتایج درمان نشان دهنده یک درمان مفید با کمترین هزینه برای عملکرد کبد است.
میکروسفرها چه هستند؟
میکروسفرها حوزه رزین که هر یک شامل میلیون ها اتم رادیواکتیو، یا (ایتریم-۹۰) می باشد. اتم های رادیواکتیو تابش کوتاه برد منتشر می کنند. هر یک از حوزه ها شامل میلیون ها اتم رادیواکتیو هستند، که حوزه با دوز تابش بالا به یک محدوده کوچک در مناطق اطراف آن است.
چگونه کار می کند؟
این روش شامل ساخت یک برش کوچک در کشاله ران تحت بی حسی موضعی، و عبورکاتتر قابل انعطاف (لوله)، به شریان کبدی از طریق شریان فمورال و سلیاک است. منابع شریان کبدی بیشترین خون را برای تومورهای کبد، با ارائه مستقیم به شریان کبدی برای اهداف انتخابی می فرستند، که با تنها درصد کمی (۱۰-۲۰٪) به بافت کبد سالم آسیب می رساند.
مداخله رادیولوژیست ممکن است برای عرضه بیشترخون از بافت کبد سالم با عبور از کاتتر به شریان کبدی چپ یا راست باشد که به شاخه های شریان اصلی کبد منجر خواهد شد. اگرتومور کبد به لوب سمت چپ یا راست کبد محدود شده باشد.
میکروسفرها ازطریق کاتتر اداره می شوند و سفر درامتداد شریان کبدی و عروق خونی کوچک واقع در اطراف سطح تومورادامه می یابد. میکروسفرها نسبتا بزرگ هستند، آنها در مویرگها تعبیه شده و مقدار زیادی از اشعه به منطقه مورد ۲-۳mm در اطراف جایی که تومورها به دام افتاده اند می فرستند. در نتیجه، هدف قراردادن تومورها ی انتخابی ، با ارائه یک دوزاز تابش بالااست، در حالی که به حداقل رساندن دوز به بافت کبد طبیعی است.
چگونه درمان تجویز می شود؟
درمان توسط دو رادیولوژیست و متخصص طب هسته ای با تجربه تایید شده برای انجام این روش است و هر دو توسط یک تیم مجرب از فیزیکدانان پزشکی، رادیولوژی، و پرستاران پشتیبانی می شوند. درمان در دو جلسه اتفاق می افتد، اولین ارزیابی قبل از درمان و در جلسه دوم، معمولا ۲ هفته بعد انجام می شد، که تحویل میکروسفرها است.
قبل از روز درمان
در روز قبل از درمان، شما دو روش تحت عنوان آنژیوگرام و اسکن پزشکی هسته ای را خواهید داشت.
آنژیوگرام یک تصویر دقیق از جزییات جریان خون به کبد را نشان می دهد، که می تواند بین افراد متفاوت باشد. قبل از آنژیوگرافی، کشاله ران با یک بی حسی موضعی بی حس و یک برش کوچک بوجود می آورند.
و سپس از طریق ، کاتتر (لوله) نرم انعطاف پذیر روی برش قرار داده و به شریان کبدی از طریق شریان فمورال (به طوری که کاتتر گاهی اوقات یک کاتتر فمورال نامیده می شود) فرستاده می شود. هنگامی که کاتتر را در محل قرار می دهند یک ماده حاجب (رنگی) است که از طریق لوله تزریق می شود تصاویر رگهای خونی با استفاده از اشعه ایکس.
یک ردیاب رادیواکتیو که تکنتیوم ۹۹m-MAA نامیده می شود، به برشی که در شریان کبدی قرار گرفته است تزریق می شود. این ردیاب رادیواکتیو یک ردیاب کم انرژی است که از رادیواکتیو میکروسفرها ی SIR با انرژی بالا تقلید می کند.
ازکبد و ریه که با یک دوربین گاما تصویربرداری شده که به تشخیص ردیاب با انرژی پایین به تیم پزشکی اجازه می دهد محل میکروسفرها را در روز درمان پیش بینی کند. این روش معمولا درحدود ۶۰-۹۰ دقیقه طول می کشد، اما ممکن است در برخی از مواردبیشتر شود. این معمولا شامل ناراحتی شما و یا ممکن است احساس گرما یا احساس سوزش خفیف هنگامی که ماده حاجب (رنگی) تزریق می شود داشته باشید. سخت ترین قسمت در این روش ممکن است دراز کشیدن به شکل صاف باشد. بعد از این روش، شما می توانید یک رژیم غذایی طبیعی داشته باشید و تمام فعالیت های عادی را درعرض ۸ تا ۱۰ ساعت از سر بگیرید.
به دنبال روش آنژیوگرافی، شما به پزشکی هسته ای برای اسکن منتقل خواهید شد. اسکن شامل با یک دوربین گاما که به تشخیص مقدار کمی ازاشعه که توسط MAA داده می شود و یک کامپیوتربرای تعیین مقدار و محل MAA جذب شده توسط بدن می شود. گاهی اوقات MAA را از طریق کبد به ریه منتقل میشود. دکتر شما باید بداند که چه مقدار از MAA با یک دوز ایمن میکروسفرهای SIR از کبد شماعبور می کند.
روز درمان
در روز درمان شما نیاز به آنژیوگرام دیگری دارید. این آنژیوگرام دوباره نیاز به یک برش کوچک در ناحیه کشاله ران با یک بی حسی موضعی دارد، به طوری که کاتتر را می توان به شریان کبدی متصل کرد. این آنژیوگرام معمولا سریعتر از درمان قبل عمل می کند. در اینجا رادیولوژیست برای شناسایی بهترین مکان برای کاتتر مداخله می کند. هنگامی که قرار دادن کاتتر تایید شد، می توان میکروسفرها را انتقال داد. این کار حدود ۱۵-۲۰ دقیقه طول می کشد. یک آرام بخش برای کمک به تسکین درد، به شما داده خواهد شد. اگر شما به آن نیاز داشته باشید. پس از عمل و تحویل میکروسفرها ،. یک پانسمان کوچک روی برش در ناحیه کشاله ران شما قرار می گیرد و فشار به محل مورد نظر برای ۱۰-۱۵ دقیقه اعمال می شود. ازشما خواسته می شود که در حدود ۴ ساعت برای جلوگیری از خونریزی دراز بکشید . بعد از آن روز و یا صبح روز بعد، شما یک اسکن پزشکی هسته ای دیگر برای قرار دادن میکروسفرها را خواهید داشت. این روش در کل ازابتدا تا انتها حدود یک ساعت طول می کشد.
حفاظت در برابر اشعه
میکروسفرها تنها برای مدت زمان محدود در رادیواکتیو باقی می مانند. پس از دو هفته بخش بسیار کوچکی از تابش اولیه باقی می ماند و بعد از ۱ ماه از تابش برای تبدیل شدن غیر قابل کشف است. میکروسفرها ی رزین در کبد به طور دائم باقی می ماند. آنها بی ضرر هستند. پیش از ترخیص، یک فیزیکدان پزشکی شما را با ارائه کاتولوگ و توضیح اقدامات احتیاطی خاص که باید انجام شود که به حداقل رساندن خطر تابش به دیگران است راهنمایی می کند. به طور معمول،به دلیل تابش کوتاه برد و طول عمر کوتاه، این اقدامات احتیاطی به حداقل رساندن (کمتر از طول بازو) و طولانی مدت (بیشتر از ۱۰ دقیقه) تماس با همکاران و یا کودکان خردسال برای هفته اول پس از آن تجویز می شود. این اقدامات احتیاطی به طور معمول می تواند به یک برنامه روزانه بدون مانع بسیار خوب تبدیل شود. یک فیزیکدان پزشکی می تواند اقدامات احتیاطی معمول قبل از درمان را مورد بحث و بررسی قرار دهد.
این رادیو دارو در درمان برخی از انواع سرطان های خون که مقاوم به درمان های دارویی هستند یا عودهای مکرر دارند، بکار می رود. این روش فاقد عوارض جانبی مانند تهوع، استفراغ سرکش و ریزش مو می باشد. برای انجام درمان با زوالین، قطع مصرف برخی از داروها توصیه می شود.
تشخیص و درمان لنفوم فولیکولار
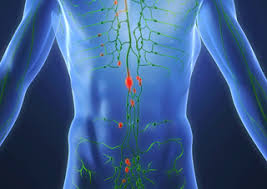
به سرطانی شدن لنفوسیت ها لنفوم می گویند. لنفوسیت یکی از انواع سلول های سفید خون می باشد که از طریق شبکه ای به نام سیستم لنفاوی در بدن گردش می کند. این سیستم شامل مغز استخوان، طحال، تیموس . غدد لنفاوی می باشد. ارگان ها و عروق لنفاوی با همکاری یکدیگر سلول هایی را تولید و ذخیره می کنند که این سلول ها وظیفه دارند با عفونت مقابله کنند.
دو نوع لنفوم وجود دارد:
– لنفوم هوچکین (HL)
– لنفوم غیر هوچکین (NHL)
لنفوم غیر هوچکین شایع ترین نوع لنفوم می باشد. لنفوم فولیکولار یکی از انواع NHL می باشد که برخلاف سایر انواع NHLها معمولا رشد آهسته ای داشته و ممکن است تا چندین سال احتیاج به درمان نداشته باشد.
در این بخش به فاکتورهای خطرساز، طبقه بندی، علائم و درمان لنفوم فولیکولار پرداخته می شود.
فاکتورهای خطرساز لنفوم فولیکولار:
سن، جنسیت و نژاد فرد در احتمال ابتلای او به لنفوم فولیکولار تاثیر گذار است. تمایل ایجاد این لنفوم در خانم ها اندکی بیشتر از مردان می باشد و در آسیایی ها و سیاه پوستان در مقایسه با نژادهای دیگر کمتر است. این لنفوم در بزرگسالان دیده می شود و میانگین سن ابتلا به آن ۶۰ سال می باشد.
علائم لنفوم فولیکولار:
اولین علامت لنفوم فولیکولار تورم یک یا چند غده ی لنفاوی بدون درد مخصوصا در ناحیه ی گردن، زیر بغل و یا کشاله ی ران می باشد. اغلب افراد مراجعه کننده با لنفوم فولیکولار از تورم طولانی مدت غدد لنفاوی شکایت دارند. قبل از شروع درمان اندازه ی این غدد لنفاوی ممکن است چندین بار افزایش یا کاهش یابد.
برخی از افراد مبتلا به لنفوم فولیکولار ممکن است توده ای را نیز در شکم خود احساس کنند. این تومور ممکن است علامتی نداشته باشد اما ممکن است سبب ایجاد انسداد در سیستم گوارشی، ادراری یا عروق خونی شود.
تشخیص و مرحله بندی لنفوم فولیکولار:
تشخیص لنفوم فولیکولار با انجام بیوپسی و برداشتن بخشی از غده ی متورم و بررسی آن در زیر میکروسکوپ تایید می شود.
پس از قطعی شدن تشخیص، آزمایش های بیشتری برای تعیین میزان تهاجم و انتشار بیماری در بدن انجام می شود. این روند، مرحله بندی نامیده می شود که در تعیین نحوه ی درمان کمک کننده خواهد بود.
شرح حال و معاینه ی فیزیکی:
معاینه ی فیزیکی دقیق در تعیین میزان گسترش بیماری کمک کننده می باشد. این معاینه می تواند غدد لنفاوی متورم را در نقاط مختلف بدن مشخص کند.
آزمایش های تعیین مرحله ی بیماری:
چندین آزمایش برای مشخص کردن نواحی از بدن که با لنفوم فولیکولار درگیر شده اند، وجود دارد که می توانند شامل موارد زیر باشند:
– تست های خونی
– بیوپسی از مغز استخوان (برداشتن نمونه ی کوچکی از بافت مغز استخوان و بررسی آن)
CT – اسکن
PET – اسکن
اصطلاحات مرحله بندی:
اصطلاحات زیر در مرحله بندی لنفوم کاربرد دارند:
منطقه ی غدد لنفاوی: غدد لنفاوی موجود در یک ناحیه به همراه بافت اطراف آن را می گویند مانند غدد لنفاوی گردنی در ناحیه ی گردن، آگزیلاری در زیر بغل، اینگوئینال در کشاله ی ران یا مدیاستینال در قفسه ی سینه.
ساختارهای لنفاوی: ارگان ها یا ساختار هایی که بخشی از سیستم لنفاوی بدن می باشند. مانند غدد لنفاوی، طحال و تیموس
دیافراگم: عضله ی بزرگی که حفره ی شکم را از فضای قفسه ی سینه جدا می کند.
مرحله بندی: مرحله بندی شامل تقسیم بیماران به گروه هایی ست که بر مبنای میزان درگیری سیستم لنفاوی در هنگام تشخیص انجام می شود. مرحله بندی به تعیین پیش آگهی و گزینه های درمانی بیمار کمک می کند.
مراحل لنفوم:
مرحله ۱: تنها غدد لنفاوی یک ناحیه یا یک ساختار لنفاوی درگیر باشد.
مرحله ۲: تعداد ۲ یا بیشتری از نواحی یا ساختارهای لنفاوی یک طرف دیافراگم درگیر باشد.
مرحله ۳: نواحی یا ساختارهای لنفاوی در دو طرف دیافراگم درگیر باشد.
مرحله ۴: ارگان ها یا بافت های دیگری غیر از نواحی یا ساختارهای لنفاوی مانند مغز استخوان درگیر باشد.
هنگامی که مرحله ی بیماری مشخص شد با توجه به این که بیمار تب، کاهش وزن یا عرق شبانه داشته باشد از حروف A یا B نیز به همراه این مراحل استفاده می شود. A به معنای عدم بروز و B به معنای بروز این علائم می باشد. به عنوان مثال فردی که با مرحله ی ۱B لنفوم مراجعه کرده باشد به معنای این است که یک منطقه ی لنفاوی در این فرد درگیر شده و او علائم B را بروز داده است.
پیشرفت لنفوم فولیکولار:
سیر پیشرفت لنفوم فولیکولار بسته به سرعت رشد تومور و ارگان های درگیر دیگر، در افراد مختلف می تواند متفاوت باشد. در برخی از افراد تا چندین سال ممکن است احتیاجی به درمان نباشد. در برخی دیگر ممکن است با بروز غلائم درمان شروع شود. این علائم می توانند شامل تب، عرق شبانه، کاهش وزن، درد، انسداد ارگان ها، کم خونی (آنمی) با تغییرات خونی دیگر باشد.
در برخی از افراد لنفوم فولیکولار ممکن است به لنفوم تهاجمی دیگری مانند DLBCL تبدیل شود که رشد سریعی داشته و احتیاج به مداخله ی درمانی فوری دارد.
درمان لنفوم فولیکولار:
درمان لنفوم فولیکولار به علائم بیماری، درجه ی تومور، سن و وضعیت سلامتی عمومی فرد بستگی دارد. اکثر افرادی که با این لنفوم مراجعه می کنند بیماری گسترش یافته ای دارند اما از آنجایی که لنفوم فولیکولار رشد آهسته ای دارد ممکن است زمان زیادی برای پیشرفت بیماری احتیاج باشد و در این دوره درمانی برای بیمار احتیاج نباشد. وقتی که علائم بیماری هنوز بروز نیافته باشد و ارگان های دیگر درگیر نشده باشند به نظر نمی رسد که درمان اولیه ی لنفوم فولیکولار بقای بیمار را بهبود بخشد. بنابراین توصیه می شود در این مرحله بیمار تحت مراقبت های دقیق واقع شود.
به علاوه آهسته بودن رشد این نوع از لنفوم پاسخ به درمان آن را کم می کند به همین دلیل اغلب این بیماری به طور کامل قابل معالجه نیست و هدف اصلی از درمان آن بهبود علائم بیمار می باشد.
ویژگی هایی که موجب می شود بیمار تحت درمان قرار گیرد می تواند شامل موارد زیر باشد:
-تورم پیشرونده ی غدد لنفاوی
– تب، کاهش وزن یا عرق شبانه
– افت سلول های خون
افرادی که علائم فوق را نداشته باشند معمولا با معاینه و آزمایش خون مرتب تحت نظر قرار می گیرند.
مراحل اولیه ی بیماری:
برخی از بیمارانی که با مرحله ی یک یا دو لنفوم فولیکولار مراجعه می کنند ممکن است با پرتو درمانی تنها درمان شوند.
پرتو درمانی: در پرتو درمانی از اشعه ی X پرانرژی برای توقف یا کاهش رشد سلول های سرطانی استفاده می شود. پرتو به غدد لنفاوی درگیر تابانده می شود. ممکن است غدد لنفاوی مجاور آنها نیز درمان شود. پرتو درمانی طی چند هفته و با دوز روزانه ی کم درمان می شود تا عوارض جانبی درمان بالا نرود. تعداد هفته های درمانی به دوز تجویزی پزشک بستگی دارد.
مرحله ی پیشرفته ی بیماری:
این مرحله شامل مراحل ۳ و ۴ لنفوم فولیکولار می باشد. گاهی اوقات مرحله ی ۲ لنفوم نیز به عنوان مرحله ی پیشرفته تلقی می شود.
گزینه های درمانی زیادی برای مرحله ی پیشرفته ی لنفوم فولیکولار وجود دارد. انتخاب نوع درمان به نظر بیمار و وضعیت بیماری فرد بستگی دارد. اکثر بیماران با این مرحله ی بیماری با داروی Rituximab و شیمی درمانی، درمان می شوند. برای بیماران مسن تری که علام بیماری را بروز داده اند اما نشانه ای از انسداد ارگان در آنها دیده نمی شود معمولا ایمنی درمانی با Rituximab توصیه می شود.
درمان با آنتی بادی: Rituximab یک آنتی بادی ست که برای درمان لنفوم فولیکولار استفاده می شود. این دارو اغلب به همراه شیمی درمانی تجویز می شود.
آنتی بادی، پروتئین خالص شده ای ست که روی سلول های خاصی اثر می گذارد. مزیت آن نسبت به درمان های دیگر مثل شیمی درمانی این است که تمامی سلول ها را تحت تاثیر قرار نمی دهد. بنابراین عوارض جانبی و خطرات طولانی مدت آن در مقایسه با شیمی درمانی کمتر می باشد.
شیمی درمانی: شیمی درمانی به استفاده از داروهایی جهت توقف یا کاهش رشد سلول های سرطانی اطلاق می شود. شمیمی درمانی روی سلول هایی که رشد سریعی دارند (مانند سلول های سرطانی) اثر گذاشته و از تقسیم یا تکثیر آنها جلوگیری می کند. از آنجایی که اکثر سلول های فرد بالغ رشد یا تکثیر زیادی ندارند کمتر تحت تاثیر داروهای شیمی درمانی قرار می گیرند به جر سلول های مغز استخوان، فولیکول های مو و مخاط مجاری گوارشی. عوارض جانبی شیمی درمانی به دلیل تاثیر این داروها بر روی ارگان های سالم بدن می باشد.
ترکیب داروهای شیمی درمانی رژیم شیمی درمانی نامیده می شود. رژیم های مورد استفاده برای درمان لنفوم فولیکولار می تواند شامل داروهای خوراکی باشد که طی یک روز مصرف می شود و یا به صورت دوره ای از طریق ورید به بیمار تزریق شود. یک دوره ی شیمی درمانی شامل زمان های تزریق دارو و فواصل استراحت بین آنها برای بهبودی بدن از عوارض جانبی ناشی از آن می باشد. به عنوان مثال یکی از رژیم های شیمی درمانی مرسوم شامل تزریق وریدی دو یا چند داروی مختلف به مدت یک ساعت می باشد که هر ۳ تا ۴ هفته انجام می شود. این دوره ی چند هفته ای یک دوره ی درمان محسوب می شود. اگر این رژیم ها ۳ یا ۴ دوره تکرار شوند درمان کامل حدود ۴ ماه به طول می انجامند.
رادیوایمونوتراپی:
رادیوایمونوتراپی (RIT) استفاده از ایزوتوپ های رادیواکتیو ذرات آلفا متصل شده به آنتی بادی می باشد در نتیجه پرتو می تواند به طور مستقیم به سمت سلول های سرطانی هدایت شود و دوز کمتری به ارگان های سالم برسد. در لنفوم فولیکولار برای انجام این درمان از Zevalin یا Bexxar استفاده می شود که به صورت وریدی تزریق می گردد. این درمان در بخش های پزشکی هسته ای بیمارستانها انجام می گیرد و پس از درمان فرد می تواند به منزل خود برگردد. تجویز رادیوایمونوتراپی احتیاج به تجهیزات ویژه و پرسنل آموزش دیده دارد.
پیوند مغز استخوان:
این درمان معمولا برای افرادی تجویز می شود که بیماری لنفوم آنها پس از درمان عود کرده باشد.
پیش آگهی لنفوم فولیکولار:
برای بیماران مبتلا به مرحله ی پیشرفته ی لنفوم فولیکولار میانگین بقای بیشتر از ۱۰ سال تخمین زده شده است. علایرغم رشد آهسته ی این بیماری اکثر افراد مبتلا به آن با درمان های موجود قابل معالجه نیستند.
محققان روشی را پیدا کرده اند که از تریق آن می توان طول عمر افراد مبتلا به لنفوم فولیکولار را تخمین زد. این روش همچنین در تعیین اثرگذاری شیمی درمانی برای این بیمارن مفید می باشد. برای این کار از ۵ فاکتور زیر استفاده می شود:
– سن بالای ۶۰ سال
– مرحله ی ۳ یا ۴ بیماری
– کاهش شمار سلول های قرمز خون
– درگیری بیش از ۵ ناحیه ی لنفاوی
– افزایش بیش از حد طیبعی سطح لاکتات دهیدروژناز خون
سرطان پستان یکی از شایعترین سرطانهای زنان است و تخمین زده میشود از هر ۹ زن یکی مبتلا به این سرطان خواهد شد. یکی از مراحل درمانی در سرطان پستان مرحله بندی زیر بغل است به این مفهوم که باید مشخص شود آیا سرطان پستان به زیر بغل و لنف نودهای آن گسترش یافته اند یا خیر. در گذشته مرحله بندی با برداشتن تمام لنف نود های زیر بغل همراه بود که عوارض بسیار زیادی از جمله لنفادم اندام را به همراه داشت. در سالهای اخیر با استفاده از مواد رادیواکتیو اولین گره لنفی در مسیر لنفاوی سرطان پستان را یافته و فقط این لنف نود را (که به گره لنفی پیشاهنگ معروف است) را برداشته و مورد بررسی قرار میدهند . در صورت عدم درگیری این لنف نود بقیه زیر بغل دست زده نمیشود. برای انجام بیوپسی گره لنفی پیشاهنگ معمولا بیمار در روز قبل از جراحی به مرکز پزشکی هسته ای مراجعه کرده و ماده رادیواکتیو در محل تومور تزریق میگردد. تصویر برداری ۳۰ دقیقه تا یک ساعت بعد محل بیوپسی گره لنفی را در زیر بغل نشان میدهد.
هدف از انجام این اسکن عمدتاً دو مورد ذیل می باشد:
بررسی مسیر درناژ لنفاوی اندامها ( دستها و پاها) و غدد لنفاوی در زمان تورم اندامها
تعیین گره پیشاهنگ در تومورها
لنفوسنتی گرافی برای تشخیص ادم لنفی اندامها (لنفادم(
لنفادم بیماری خاص دستگاه لنفی بدن است که به صورت تورم اندامها (دستها و پاها) خود را نشان میدهد و معمولا به دنبال جراحی های زیر بغل یا کشاله ران اتفاق می افتد ولی انواع اولیه (بدون علت مشخص) آن هم وجود دارد.
لنفادم اولیه معمولا در سنین جوانی اتفاق افتاده و با تورم پیشرونده اندامها همراه است. افتراق این بیماری از سایر علت تورم اندامها بسیار مهم است.
لنفوسینتی گرافی یک روش بسیار ساده برای تشخیص قطعی لنفادم است. در این روش مقدار اندکی ماده رادیو اکتیو در بین انگشتان دست یا پا تزریق شده و تصویربرداری از بیمار حدود یک ساعت بعد انجام میشود. این روش میتواند در تشخیص و پیگیری لنفادم کمک شایانی بکند.
اطلاعات زمینه ای
آلودگی میکروبی مخاط معده با هلیکوباکترپیلوری، یکی از علل شایع زخم معده است. درمان صحیح این عفونت باعث رفع علائم بیماری در فرد مبتلا می شود. بهترین تست برای ارزیابی اثر درمان و ریشه کن شدن این عفونت، تست تنفسی UBT می باشد که معمولاً حدود ۲ هفته پس از یک دوره درمانی تحت نظر پزشک، انجام می گیرد. در مرکز پزشکی هسته ای دکتر کاظمی، این تست با استفاده از روش PYtest که تنها تست تنفسی با تأییدیه FDA می باشد و استفاده از آن را در کودکان و زنان باردار و شیرده مجاز شمرده است، با دقت ۱۰۰% انجام می شود. برای انجام این تست که تنها با دمیدن در یک بالن، ۱۰ دقیقه پس از خوردن کپسول حاوی کربن ۱۴ صورت می-گیرد، لازم است بیمار ۴ ساعت ناشتا بوده و از مصرف آنتی بیوتیک ها به مدت یک هفته، خودداری نماید.
تست تنفسی اوره آز UBT
عفونت هلیکوباکتر پیلوری H. Pylori از گسترده ترین عفونت های انسانی بدون محدودیت سن و جنس است. انسان از میزبانان اصلی این باکتری بوده و بیماری از راه دهان به دهان یا مدفوع به دهان انتقال می یابد. رشد میکروب H. Pylori در معده به طور بالقوه عامل گاستریت (ورم معده) مزمن و زخم معده می باشد. این میکروب شایعترین علت گاستریت مزمن است که تقریبا در ۱۰۰ % بیماران مبتلا به زخم اثنی عشر و ۸۰ % بیماران مبتلا به زخم معده تشخیص داده شده و بعنوان عامل خطر برای پیشرفت تومور معده و سرطان معده شناخته شده است. عفونت به آرامی و بدون علامت پیشرفت کرده و در بسیاری از بیماران فاقد علائم بالینی است. آزمایشات تشخیصی عفونت هلیکوباکتر به دو دسته تست نیازمند به آندوسکوپی (تهاجمی) و غیر نیازمند به آندوسکوپی (غیر تهاجمی) تقسیم می شوند. تصمیم گیری در مورد انتخاب آزمایش مناسب در شرایط مختلف بستگی به میزان لزوم بررسی بیمار توسط آندوسکوپی فوقانی و همچنین آگاهی ازنقاط ضعف و قدرت آزمایشات مختلف دارد. آزمایش آندوسکوپی با توجه به هزینه بالای آن تنها باید در مواردی انجام شود که انجام آن از نظر بالینی به دلایل دیگری ضروری باشد و اگر پیگیری آندوسکوپی ضرورت نداشته باشد از روش های غیر تهاجمی استفاده می شود.
روش های تشخیصی غیر از آندوسکوپی عبارتند از:
– آزمایش سرولوژی (آنتی بادی)
– تست اوره تنفسی
آزمایش سرولوژی نمی تواند میان یک عفونت فعال که باعث بیماری می شود و یک عفونت نهفته که علائمی ایجاد نمی کند، تفاوتی قائل شود. همچنین این آزمایش نمی تواند بگوید که آیا درمان باعث معالجه بیماری و ریشه کنی باکتری شده است یا نه، چرا که پادتن های ضد باکتری مدتها پس از نابودی آن در خون باقی می مانند. با توجه به حساسیت پایین و محدودیتهای تست های سرولوژیک برای ارزیابی عفونت فعال،بهترین روش تست اوره تنفسی می باشد. این تست که براساس فعالیت آنزیم اوره آز (C-14-urea) می باشد، یک شیوه سریع، ایمن و دقیق برای شناسایی هلیکوباکتر پیلوری است و از آنجایی که تنها باکتری های فعال را شناسایی میکند، علاوه بر تشخیص در بررسی میزان تاثیر درمان نیز قابل استفاده می باشد. همچنین این تست برای جمعیت های مختلف شامل کودکان، زنان باردار و شیرده، افراد مسن و بیمارانی که نمی توانند آندوسکوپی را تحمل کنند استفاده می شود.
فرایند انجام تست:
ابتدا کپسول خوراکی حاوی یک میکروکوری اوره نشاندار به کربن۱۴ (C-14-urea) توسط بیمار خورده می شود. حدود ۱۵ دقیقه بعد بیمار شروع به تنفس در کیسه مخصوص به نام کارت تنفسی می کند.سپس کارت تنفسی در دستگاه UBT قرارداده شده و نتایج تست مشخص می گردد. اگر هلیکوباکتر پیلوری در معده وجود داشته باشد با مصرف اوره نشاندار باعث تولید آمونیاک و دی اکسید کربن نشاندار می شود که در هوای بازدمی قابل شناسایی است.
مدت زمان انجام: حدود ۱ ساعت
آمادگی های انجام تست اوره تنفسی:
– بیمار باید به مدت ۴ تا ۶ ساعت ناشتا باشد.
– از یک ماه قبل آنتی بیوتیک های خوراکی و قرص بیسموت قطع شود.
– از ۱۵ روز قبل امپرازول (امکس) و پانتزول (پانتپرازول) و لانزوپرازول قطع شود.
– از ۴۸ ساعت قبل قرص های سایمتیدین و رانیتیدین قطع شود.
– از ۴۸ ساعت قبل سیگار و قلیان نکشید.
– مسواک شخصی خود را همراه بیاورید.